Dysprosium,Symbol Dy und Ordnungszahl 66. Es ist einSeltenerdelementmit metallischem Glanz. Dysprosium wurde in der Natur nie als einzelne Substanz gefunden, obwohl es in verschiedenen Mineralien wie Yttriumphosphat vorkommt.

Die Häufigkeit von Dysprosium in der Kruste beträgt 6 ppm und ist damit niedriger als die von
Yttriumin schweren Seltenen Erden. Es gilt als relativ häufiges schweres
Seltenerdelement und bietet eine gute Ressourcengrundlage für seine Anwendung.
Dysprosium besteht in seinem natürlichen Zustand aus sieben Isotopen, wobei 164 Dy das am häufigsten vorkommende ist.
Dysprosium wurde erstmals 1886 von Paul Achilleck de Bospoland entdeckt, konnte aber erst mit der Entwicklung der Ionenaustauschtechnologie in den 1950er Jahren vollständig isoliert werden. Dysprosium hat relativ wenige Anwendungen, da es nicht durch andere chemische Elemente ersetzt werden kann.
Lösliche Dysprosiumsalze sind leicht toxisch, während unlösliche Salze als ungiftig gelten.
Geschichte entdecken
Entdeckt von: L. Boisbaudran, Franzose
1886 in Frankreich entdeckt
Nach der Trennung von MossanderErbiumErde undTerbiumAls 1842 Yttriumerde von Yttriumerde getrennt wurde, nutzten viele Chemiker Spektralanalysen, um festzustellen, dass es sich nicht um reine Oxide eines Elements handelte. Dies ermutigte Chemiker, weiterhin an deren Trennung zu arbeiten. Sieben Jahre nach der Trennung von Holmium, im Jahr 1886, teilte Bouvabadrand es in zwei Hälften und behielt Holmium bei. Die andere Hälfte erhielt den Namen Dysprosium mit dem Elementsymbol Dy. Dieses Wort stammt vom griechischen Wort dysprositos und bedeutet „schwer zu erhalten“. Mit der Entdeckung von Dysprosium und anderen Seltenerdelementen wurde die zweite Hälfte der dritten Phase der Seltenerdelement-Entdeckung abgeschlossen.
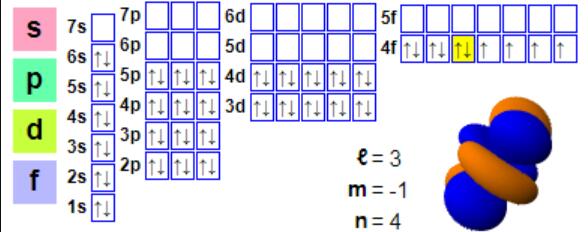
Elektronenkonfiguration
Elektronisches Layout:
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f10
Isotop
In seinem natürlichen Zustand besteht Dysprosium aus sieben Isotopen: 156Dy, 158Dy, 160Dy, 161Dy, 162Dy, 163Dy und 164Dy. Sie gelten alle als stabil, trotz des 156Dy-Zerfalls mit einer Halbwertszeit von über 1 * 1018 Jahren. Unter den natürlich vorkommenden Isotopen ist 164Dy mit 28 % das häufigste, gefolgt von 162Dy mit 26 %. Am wenigsten verbreitet ist 156Dy mit 0,06 %. Es wurden außerdem 29 radioaktive Isotope synthetisiert, deren Atommasse zwischen 138 und 173 liegt. Das stabilste Isotop ist 154Dy mit einer Halbwertszeit von etwa 3106 Jahren, gefolgt von 159Dy mit einer Halbwertszeit von 144,4 Tagen. Am instabilsten ist 138 Dy mit einer Halbwertszeit von 200 Millisekunden. 154 Dy wird hauptsächlich durch Alphazerfall verursacht, während der Zerfall von 152 Dy und 159 Dy hauptsächlich durch Elektroneneinfang verursacht wird.
Metall
Dysprosium hat einen metallischen und einen hellen Silberglanz. Es ist relativ weich und lässt sich funkenfrei bearbeiten, sofern Überhitzung vermieden wird. Die physikalischen Eigenschaften von Dysprosium werden bereits durch geringe Mengen an Verunreinigungen beeinflusst. Dysprosium und Holmium haben die höchste magnetische Stärke, insbesondere bei niedrigen Temperaturen. Ein einfacher Dysprosium-Ferromagnet nimmt bei Temperaturen unter 85 K (-188,2 °C) und über 85 K (-188,2 °C) einen helikalen antiferromagnetischen Zustand an, in dem alle Atome zu einem bestimmten Zeitpunkt parallel zur untersten Schicht ausgerichtet sind und benachbarten Schichten in einem festen Winkel gegenüberstehen. Dieser ungewöhnliche Antiferromagnetismus geht bei 179 K (-94 °C) in einen ungeordneten (paramagnetischen) Zustand über.
Anwendung:
(1) Als Zusatz für Neodym-Eisen-Bor-Dauermagnete kann die Zugabe von etwa 2–3 % Dysprosium zu diesem Magnettyp dessen Koerzitivfeldstärke verbessern. In der Vergangenheit war die Nachfrage nach Dysprosium gering, doch mit der steigenden Nachfrage nach Neodym-Eisen-Bor-Magneten wurde es zu einem notwendigen Zusatzelement mit einem Gehalt von etwa 95–99,9 %, und die Nachfrage steigt ebenfalls rasant.
(2) Dysprosium wird als Aktivator für Leuchtstoffe verwendet. Dreiwertiges Dysprosium ist ein vielversprechendes Aktivierungs-Ion für dreifarbige Leuchtstoffe mit einem einzigen Emissionszentrum. Es besteht hauptsächlich aus zwei Emissionsbändern: einem gelben und einem blauen. Mit Dysprosium dotierte Leuchtstoffe können als dreifarbige Leuchtstoffe verwendet werden.
(3) Dysprosium ist ein notwendiger metallischer Rohstoff für die Herstellung der großen magnetostriktiven Legierung Terfenol, die präzise mechanische Bewegungen ermöglichen kann.
(4)Dysprosiummetall kann als magnetooptisches Speichermaterial mit hoher Aufzeichnungsgeschwindigkeit und Leseempfindlichkeit verwendet werden.
(5) Zur Herstellung von Dysprosiumlampen wird Dysprosiumiodid als Arbeitsstoff verwendet. Dieser Lampentyp bietet Vorteile wie hohe Helligkeit, gute Farbe, hohe Farbtemperatur, geringe Größe und einen stabilen Lichtbogen. Er wird als Lichtquelle für Filme, Drucke und andere Beleuchtungsanwendungen eingesetzt.
(6) Aufgrund seines großen Neutroneneinfangquerschnitts wird Dysprosium in der Atomindustrie zur Messung von Neutronenspektren oder als Neutronenabsorber eingesetzt.
(7) Dy3Al5O12 kann auch als magnetischer Arbeitsstoff für die magnetische Kühlung verwendet werden. Mit der Entwicklung von Wissenschaft und Technologie werden sich die Anwendungsgebiete von Dysprosium weiter ausweiten.
(8) Dysprosium-Verbindungsnanofasern weisen eine hohe Festigkeit und Oberfläche auf und können daher zur Verstärkung anderer Materialien oder als Katalysatoren eingesetzt werden. Durch Erhitzen einer wässrigen Lösung aus DyBr3 und NaF bei 450 bar Druck für 17 Stunden auf 450 °C können Dysprosiumfluoridfasern erzeugt werden. Dieses Material kann in verschiedenen wässrigen Lösungen bei Temperaturen über 400 °C über 100 Stunden verbleiben, ohne sich aufzulösen oder zu verklumpen.
(9) In Wärmedämm-Entmagnetisierungskühlschränken werden bestimmte paramagnetische Dysprosiumsalzkristalle verwendet, darunter Dysprosium-Gallium-Granat (DGG), Dysprosium-Aluminium-Granat (DAG) und Dysprosium-Eisen-Granat (DyIG).
(10) Verbindungen der Dysprosium-Cadmiumoxid-Gruppe sind Infrarotstrahlungsquellen, die zur Untersuchung chemischer Reaktionen eingesetzt werden können. Dysprosium und seine Verbindungen besitzen starke magnetische Eigenschaften und eignen sich daher gut für Datenspeicher wie Festplatten.
(11) Der Neodym-Anteil von Neodym-Eisen-Bor-Magneten kann durch Dysprosium ersetzt werden, um die Koerzitivfeldstärke zu erhöhen und die Hitzebeständigkeit der Magnete zu verbessern. Dysprosium wird in Anwendungen mit hohen Leistungsanforderungen eingesetzt, beispielsweise in Antriebsmotoren von Elektrofahrzeugen. Fahrzeuge mit diesem Magnettyp können bis zu 100 Gramm Dysprosium pro Fahrzeug enthalten. Da Toyota jährlich zwei Millionen Fahrzeuge absetzt, wird der weltweite Vorrat an Dysprosiummetall bald erschöpft sein. Durch Dysprosium ersetzte Magnete weisen zudem eine hohe Korrosionsbeständigkeit auf.
(12) Dysprosiumverbindungen können als Katalysatoren in der Ölraffination und der chemischen Industrie eingesetzt werden. Wird Dysprosium als Strukturvermittler in einem Ferrioxid-Ammoniak-Synthesekatalysator eingesetzt, können dessen katalytische Aktivität und Hitzebeständigkeit verbessert werden. Dysprosiumoxid kann als dielektrisches Hochfrequenz-Keramikbauteilmaterial mit einer Mg₂-Ba₂-Dy₂n-Ti₂-Struktur verwendet werden und eignet sich für dielektrische Resonatoren, dielektrische Filter, dielektrische Diplexer und Kommunikationsgeräte.
Veröffentlichungszeit: 23. August 2023